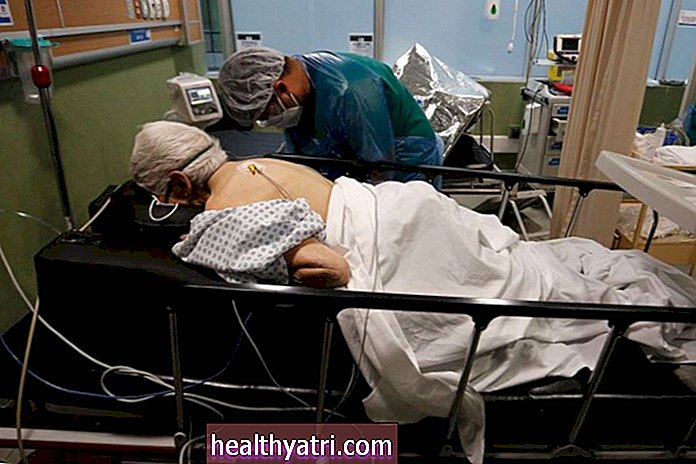
신종 코로나 바이러스 (COVID-19)는 전 세계적으로 수백만 명의 사람들을 감염시킨 유행병으로 발전했습니다. 과학자와 연구자들은 질병에 대한 치료법을 찾기 위해 적극적으로 노력하고 있으며, 이상적으로는 처음부터 감염을 예방할 수있는 방법을 찾고 있습니다.
Geber86 / 게티 이미지기존 약물, 신약의 잠재적 효과를 평가하고 백신 및 혈액 제품의 생존 가능성을 테스트하는 수백 개의 임상 시험이 진행 중입니다. 다음은 현재 임상 사용중인 것부터 아직 조사중인 것까지 바이러스에 대해 테스트 된 주요 치료법의 목록입니다.
2020 년 12 월 현재 미국 식품의 약국 (FDA)의 응급 사용 승인을받은 9 가지 치료제 : 렘 데시 비르 (2020 년 5 월), 회복기 혈장 (2020 년 8 월), 밤 라니 비맙 단일 클론 항체 (2020 년 11 월), 바리 시티 닙 결합 remdesivir (2020 년 11 월), 결합 된 casirivimab 및 imdevimab 단일 클론 항체 (2020 년 11 월), Pfizer-BioNTech mRNA 백신 (2020 년 12 월), Moderna mRNA 백신 (2020 년 12 월), 결합 된 bamlanivimab 및 etesevimab 단일 클론 항체 (2021 년 2 월) 및 Johnson & Johnson 아데노 바이러스 벡터 백신 (2021 년 2 월).
렘 데시 비르
Remdesivir는 처음에 에볼라에 대한 치료제로 개발되었습니다. 체외 연구에 따르면 COVID-19에 효과적 일 수 있다는 사실이 밝혀진 후, 동정심 많은 사용 요청을 통해 병원은 중증 환자 치료를 위해 약물에 접근 할 수있었습니다. 5 월 1 일, FDA로부터 응급 사용 허가를받은 COVID-19의 첫 번째 치료 옵션이되었습니다. FDA는 중증 질환으로 입원 한 성인과 어린이에게 사용하도록 허용했습니다. 10 월 22 일, remdesivir는 응급 사용 허가없이 COVID-19를 치료하기 위해 FDA가 승인 한 최초의 약물이되었습니다. 11 월 19 일에는 바리 시티 닙과 함께 사용할 때 새로운 EUA 승인을 받았습니다 (아래 Biologics 참조).
연구 결과
에 발표 된 연구뉴 잉글랜드 의학 저널입원 한 COVID-19 환자를 대상으로 한 61 명의 렘 데시 비르 치료 사용 사례를 조사했습니다. 이 환자들은 심하게 아팠습니다. 연구를 시작할 때 30 명은 기계 환기에, 4 명은 체외 막 산소화 (ECMO)에있었습니다. 평균 18 일 동안 환자의 68 %가 산소 공급이 개선되었으며 인공 호흡기를 사용하는 사람들의 57 %가 발관을 할 수있었습니다. 그러나 60 %는 부작용이 있었으며 23 %의 사람들 (모두 기계 환기 그룹)은 다발성 기관 기능 장애 증후군, 패 혈성 쇼크, 급성 신장 손상 및 저혈압을 포함한 심각한 합병증을 앓았습니다.
NIH (National Institutes of Health)의 임상 시험 인 적응 형 COVID-19 치료 시험 (ACTT)에서 약물로 치료 한 중증 COVID-19 감염 환자의 증상이 4 일 더 빨리 개선되는 것으로 나타났습니다 (31 % 더 빠름). 치료받지 않은 사람들보다. 전체 생존율이 개선 된 것처럼 보였지만 통계적으로 유의미하지는 않았습니다. 그러나 중등도 감염 환자는 10 일간의 렘 데시 비르로 치료했을 때 표준 치료에 비해 크게 개선되지 않았습니다. 5 일간의 렘 데시 비르 치료로 치료받은 사람들에게 개선이 있었지만 연구자들은 "그 차이가 임상 적으로 중요하지 않다는 점을 지적했습니다.
의약품 제조업체 인 Gilead Sciences가 발표 한 데이터는 무작위 대조 시험에서 개선 된 임상 결과를 언급했습니다. COVID-19로 입원 한 사람들은 렘 데시 비르 (n = 541) 또는 위약 (n = 521)으로 10 일 동안 치료를 받았습니다. 치료 그룹의 사람들은 대조군에있는 사람들보다 5 일 더 빨리 회복되었고, 산소 지원 기간이 더 짧았으며, 더 빨리 퇴원 할 가능성이 더 높았습니다.
대조적으로, 세계 보건기구 (WHO)는 그들의 연대 시험에서 임상 적 이점을 발견하지 못했습니다. 이 연구에는 30 개국에서 COVID-19로 입원 한 거의 11,300 명이 포함되었습니다. 연구 참가자는 hydroxychloroquine, interferon, lopinavir-ritanovir 또는 remdesivir의 네 가지 치료법 중 하나를 받았습니다. 어떤 치료도 28 일 동안 사망률을 감소시키지 않았거나 인공 호흡기 치료를 시작해야 할 필요성이 없었습니다. 그 이후로 WHO는 입원 환자에게 약물 사용을 공식적으로 금지했습니다. Gilead Sciences는 이러한 결과에 이의를 제기했으며 동료 검토가 보류 중입니다.
국립 보건원은 기존의 산소 요법이 필요한 입원 COVID-19 환자에게 remdesivir, dexamethasone 또는 remdesivir와 dexamethasone의 조합을 권장합니다.
덱사메타손 및 메틸 프레드니솔론
Dexamethasone과 methylprednisolone은 염증 치료에 자주 사용되는 스테로이드입니다. 그들은 경구 및 IV 제형으로 제공됩니다. COVID-19는 많은 경우에 심각한 염증 반응과 관련이 있으며 연구자들은 이러한 일반적인 항염증제 사용의 이점을 조사했습니다.
연구 결과
RECOVERY 시험 (COVid-19 thERapY의 무작위 평가) 시험은 10 일에 걸쳐 매일 1 회 덱사메타손으로 치료하면 위약과 비교할 때 임상 결과가 개선되었음을 발견했습니다. 특히, 인공 호흡기를 착용 한 환자의 사망률은 41 %에서 29 %로, 인공 호흡기 치료없이 산소가 필요한 환자의 경우 26 %에서 23 %로 감소했습니다. 산소 나 인공 호흡기 요법이 필요하지 않은 환자는 덱사메타손의 임상 적 이점을 보지 못했습니다.
세계 보건기구 (WHO)가 후원하는 메타 분석은 약 1,700 명의 중증 COVID-19 환자를 포함한 7 개의 무작위 임상 시험을 검토했습니다. 에 게시JAMA,이 연구는 스테로이드 (덱사메타손, 하이드로 코르티손 또는 메틸 프레드니솔론)로 치료받은 사람들의 28 일 사망률이 일반적인 치료 또는 위약으로 치료받은 사람들 (스테로이드의 절대 사망률 32 % 대 대조군의 경우 40 %)보다 훨씬 낮다는 것을 발견했습니다. .
스테로이드는 토 실리 주맙과 함께 사용할 때 이점이 있습니다 (아래의 생물 제제 섹션 참조). 연구류마티스 질환 연대기체내 과민성 염증 증후군 인 사이토 카인 폭풍이있는 COVID-19 환자를 평가했습니다. COVID-19 및 사이토 카인 폭풍에 걸린 환자는 5 일 동안 고용량 글루코 코르티코이드 인 메틸 프레드니솔론으로 치료 받았습니다. 2 일 이내에 임상 개선이 시작되지 않으면 토 실리 주맙 IV도 투여 받았습니다. 지지 요법으로 치료받은 사람들과 비교할 때 치료 그룹은 7 일 동안 호흡기 증상이 임상 적으로 개선 될 가능성이 79 % 더 높았고, 병원에서 사망 할 가능성이 65 % 적 었으며, 기계적 환기가 필요할 가능성이 71 % 낮았습니다. 또 다른 연구는가슴, COVID-19로 입원 한 5,776 명의 환자에게서 발견 된 복합 요법의 이점을 확인했습니다. 코르티코 스테로이드는 사망률을 34 % 감소 시켰지만 토 실리 주맙과 병용했을 때 사망률은 56 % 감소했습니다.
소아에서 다 계통 염증 증후군 (MIS-C)이 발생하는 소아는 메틸 프레드니솔론의 혜택을받을 수 있습니다.JAMA. 이 연구에서, 증후군을 앓고있는 111 명의 어린이가 메틸 프레드니솔론을 포함하거나 포함하지 않은 IV 면역 글로불린으로 치료를 받았습니다. 두 치료를 모두받은 소아는 결과가 개선되었으며, 특히 2 일 이내에 열이 감소하고 7 일 동안 열 재발이 감소했습니다.
회복기 플라즈마
약물은 COVID-19를 표적으로 삼는 한 가지 방법이지만 우리 몸도 질병에 대처할 수있는 방법을 제공 할 수 있습니다. COVID-19와 같은 이물질에 노출되면 면역 체계가 이에 대한 항체를 생성 할 수 있습니다. 이러한 항체를 포함하는 혈액을 회복기 혈장이라고합니다.
아픈 사람에게서 혈장을 제거하고 COVID-19에서 회복 된 사람의 회복기 혈장으로 대체하면 감염과 싸우는 데 도움이 될 수 있습니다. 이 과정을 플라즈마 교환이라고합니다.
연구 결과
두 개의 소규모 연구에서 중증 감염 사례를 치료하기 위해 회복기 혈장을 사용하는 것이 잠재적 인 이점을 보여주었습니다. 한 사례 시리즈에는 기계적 환기가 필요한 중증 폐렴 환자 5 명이 포함되었습니다. 별도의 파일럿 연구에는 중증 COVID-19 감염 환자 10 명이 포함되었습니다. 모든 환자는 회복기 혈장으로 수혈을 받았다. 두 연구 모두 3 일 이내에 증상이 개선되고 2 주 이내에 바이러스 부하가 감소한 것으로 나타났습니다 (케이스 시리즈의 경우 12 일, 파일럿 연구의 경우 7 일). 그러나 인공 호흡기를 끊는 능력은 느 렸고 모든 환자에게 달성되지 않았습니다. 가장 중요한 것은 치료로 인한 피해가없는 것 같습니다.
2020 년 4 월 FDA는 존스 홉킨스 메디슨에서 진행 한 무작위 위약 대조 임상 시험 2 건을 승인하여 혈장이 중증 감염자뿐만 아니라 COVID-19 감염 예방에 도움이 될 수 있는지 확인했습니다.
결과는 다양했습니다. 긍정적 인 점에서메이요 클리닉 절차20,000 명의 입원 한 COVID-19 환자를 치료하는 데 사용되었을 때 회복기 혈장은 일반적으로 안전 할뿐만 아니라, 특히 질병의 초기에 투여되었을 때 사망률 감소와 관련이있을 수 있습니다. 현재까지 가장 큰 시험은 35,000 명 이상의 입원 환자를 회복기 혈장으로 치료했습니다. 이 발견은 높은 항체 수치를 가진 혈장 치료는 진단 후 3 일 이내에 투여하면 사망률을 낮추는 것으로 나타났습니다. 160 명의 COVID-19 환자를 대상으로 한 연구에 따르면 65 세 이상의 노인을 경미한 증상 3 일 이내에 치료하면 15 일 동안 중증 호흡기 질환으로 진행될 위험이 절반 (치료시 16 %, 위약 사용시 31 %) 감소했습니다. 연구에서 사망률은 평가되지 않았지만 연구원들은 성인 1 명의 심각한 질병을 줄이기 위해 7 명의 노인 만이 치료를 받아야한다고 추정했습니다.
모든 연구가 그렇게 유리한 것은 아닙니다. 거의 500 명의 성인을 대상으로 한 연구에 따르면 회복기 혈장은 7 일 이내에 바이러스 부하를 줄 였지만 사망률은 감소하지 않았습니다. COVID-19 폐렴을 앓고있는 228 명의 성인을 대상으로 한 무작위 대조 연구에서 30 일 동안 회복기 혈장으로 치료받은 사람들에게 임상 적 이점이 없음을 발견했습니다. 국립 보건원 (National Institutes of Health)은 경증에서 중등도의 COVID 증상이있는 사람들에게 혜택이 없다는 점을 지적하면서 2021 년 3 월 임상 시험을 중단했습니다.
더 일관 적이거나 강력한 데이터 없이는 2020 년 8 월 COVID-19 치료제로 회복기 혈장에 대한 FDA의 긴급 승인에 대한 논란이있었습니다. 2020 년 2 월 EUA가 업데이트되었습니다. 항체 역가가 높은 회복기 혈장 만 현재 사용이 승인되었습니다. 또한 질병 초기에 입원 한 환자 나 면역력이 약한 입원 환자로 제한되었습니다.
회복기 혈장은 헌혈처럼 수집 할 수 있으며, 혈장에 감염이 없음을 확인하기위한 기술이 수행됩니다. 현재 혈장을 기증하기 전 최소 2 주 동안 증상이없는 사람이있는 것이 좋습니다.
수십 개의 미국 병원이 현재 전국 COVID-19 회복기 플라즈마 프로젝트에 참여하여 치료 용 혈장 교환을 조사하기 위해 협력하고 있습니다.
Regeneron Pharmaceuticals —Casirivimab 및 Imdevimab (이전 REGN-COV2)
Regeneron Pharmaceuticals Inc.는 처음에는 REGN-COV2라고 불리는 인공 항생제 칵테일을 개발했으며, 현재는 casirivimab 및 imdevimab으로 알려져 있습니다. 연구 치료에는 COVID-19에 대한 두 가지 항체가 포함됩니다. 회사는 치료 7 일 이내에 바이러스 부하와 COVID-19 증상이 감소했음을 시사하는 예비 데이터를 발표했습니다. 임상 시험에 524 명을 추가 한 후 REGN-COV2는 위약으로 치료받은 사람들과 비교했을 때 29 일까지 COVID 관련 의료 방문의 필요성을 줄이는 것으로 나타났습니다 (2.8 % 대 6.8 %). 이 그룹에서 "불합리한 위험 / 이점 프로파일"에 근거하여 고 유량 산소 또는 기계적 환기가 필요한 사람들에 대한 시험은 보류되었습니다. 10 월 1 일 코로나 19 검사 결과 양성을보고 한 도널드 트럼프 대통령은 2020 년 10 월 2 일 REGN-COV2 치료를 받았다.
11 월 21 일 FDA는 합병증 위험이 높고 입원하지 않고 산소 보충이 필요하지 않은 경증에서 중등도 질환이있는 COVID-19 환자를 위해 항체 칵테일에 대한 긴급 사용 허가를 부여했습니다. 그러나 국립 보건원은 "경증에서 중등도의 COVID-19에 걸린 외래 환자의 치료를 위해 카시 리비 맙과 임 데비 맙의 사용을 권장하거나 반대 할 데이터가 충분하지 않기 때문에이 치료가 표준 치료가되어서는 안된다"고 말합니다.
Regeneron은 Casirivimab-imdevimab 칵테일이 고위험에 노출 된 사람들의 COVID-19 감염을 감소 시켰다고 발표 한 3 상 시험 결과를 보도 자료로 발표했습니다. 이 연구는 400 명을 무작위로 치료 또는 위약으로 선정했습니다. 칵테일을받은 사람 (n = 186)은 증상이있는 감염이 발생하지 않았지만 10 명은 무증상 감염이 발생했습니다. 그러나 위약 그룹 (n = 223)에서는 8 건의 증상 감염과 23 건의 무증상 감염이 발생했습니다. 전체적으로 치료는 모든 COVID-19 감염률을 절반으로 줄였으며 (치료군 5 %, 위약 10 %) 증상이있는 감염으로부터 완전히 보호되었습니다.
기타 합성 항체
Regeneron Pharmaceuticals Inc.가 실험실에서 제조 된 합성 항체의 효과를 조사하려는 유일한 회사는 아닙니다.
Eli Lilly — Bamlanivimab
National Institute of Allergy and Infectious Diseases가 부분적으로 후원 한 Eli Lilly and Company는 COVID-19를 중화시키기위한 단일 클론 항체 (처음에는 bamlanivimab으로 명명 된 이후 LY-CoV555로 알려짐)를 개발했습니다. 임상 2상은 452 명을 각각 3 회 투여했습니다. 두 번째 투여 후 바이러스 부하가 감소했지만 치료 및 위약 그룹은 세 번째 투여 후 비슷한 바이러스 부하를 가졌습니다. 그러나 치료는 2 일부터 6 일까지 증상의 심각성을 감소 시켰고 29 일에 병원에 남아있는 사람들의 수를 감소 시켰습니다 (1.6 % 대 6.3 %). 연구는 ACTIV-3- 시험에서 3 상 임상 시험과 렘 데시 비르 병용 치료로 진행되었습니다. 그러나 10 월 13 일, 치료에 대한 불특정 한 안전성 우려가 제기되어 입원 환자에 대한 임상 시험이 보류되었습니다.
11 월 9 일 FDA는 경증에서 중등도의 COVID-19를 앓고 입원하지 않고 COVID-19 감염으로 인해 산소 요법이 필요하지 않은 고위험 사람들을 위해이 치료에 대한 응급 사용 허가를 발표했습니다.
12 월에 경증에서 중등도의 COVID-19 환자 314 명을 대상으로 한 연구가뉴 잉글랜드 의학 저널. 모든 연구 참가자는 렘 데시 비르와 적절한 경우 산소 및 / 또는 덱사메타손으로 치료를 받았습니다. 그런 다음 그들은 bamlanivimab 또는 위약을 받기 위해 무작위로 배정되었습니다. 연구원들은 중화 항체로 치료받은 사람들이 5 일째까지 호흡기 증상을 개선하지 못했다고 지적했습니다. 연구는 효과가 없어 모집을 중단했습니다.
보도 자료에서 Eli Lilly는 예방 요법으로 bamlanivimab의 효과를보고했습니다. BLAZE-2 시험 (결과는 아직 발표되지 않음)에서 처음에 COVID-19에 대해 음성 판정을받은 965 명의 요양원 거주자는 단일 클론 항체 또는 위약으로 치료를 받았습니다. 8 주 동안 밤 라니 비맙으로 치료받은 사람들은 증상이있는 COVID-19에 걸릴 확률이 57 % 낮았습니다. 4 명이 감염으로 사망했지만 치료군에는 없었습니다.
2020 년 2 월 FDA는 단클론 항체 인 bamlanivimab과 etesevimab의 조합에 대한 응급 사용 허가를 승인했습니다. 이 치료는 산소 보충이 필요하지 않은 경증에서 중등도의 COVID-19 증상이있는 입원하지 않은 환자를 대상으로합니다. 환자는 12 세 이상, 체중 40kg 이상이어야하며 고위험으로 간주되어야합니다 (예 : 65 세 이상, 특정 만성 질환이있는 경우 등). 1,035 명을 대상으로 한 무작위 이중 맹검 위약 대조 임상 시험 연구에서이 치료를받은 사람들은 COVID-19로 인해 입원하거나 사망 할 가능성이 낮았습니다 (2 % 대 7 %).
3 상 임상 시험은 769 명의 COVID-19 환자를 단일 클론 항체 조합 또는 위약으로 치료했습니다. 모든 참가자는 12 세 이상이었으며 고위험군으로 간주되었으며 경증에서 중등도의 증상을 보였으며 연구 시작시 입원하지 않았습니다. 치료 그룹의 4 명은 결국 입원 (4/511)이 필요했고, 위약 그룹의 15 명은 입원했으며, 그중 4 명은 사망 (15/258)했습니다. 전체적으로 bamlanivimab-etesevimab 조합은 입원 또는 사망 위험을 87 % 감소 시켰습니다.
AstraZeneca — AZD7442
AstraZeneca는 임상 3 상을 시작하여 조사 항체 (AZD7442)가 COVID-19 감염을 치료하고 예방할 수 있는지 확인합니다. 전임상 연구에서 생쥐에서 효과가 나타났습니다. 아직 임상 적으로 사용하고 있지 않습니다.
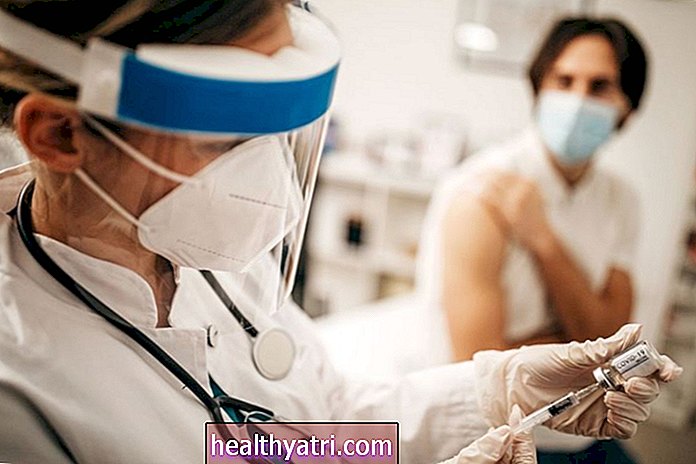
COVID-19 백신
COVID-19를 장기간 관리하기위한 최선의 희망은 백신을 개발하는 것입니다. 백신은 신체를 항원 (이 경우 바이러스로부터 면역 반응을 일으키는 물질)에 노출시키고 면역 체계에서 항체 생성을 유발합니다. 목표는 감염을 일으키지 않고 바이러스에 대한 항체를 만드는 것입니다. 그렇게하면 그 항원에 다시 노출되면 신체는 그 항원에 대한 항체를 만드는 방법을 기억하게됩니다. 바라건대, 면역 반응이 너무 강해서 전혀 아프지 않을 것입니다. 그러나 병에 걸리면 예방 접종을 맞지 않은 경우보다 증상이 가벼워집니다.
COVID-19 백신 : 어떤 백신이 사용 가능한지, 누가 백신을 맞을 수 있는지, 얼마나 안전한지 최신 상태로 유지하십시오.
6 개의 주요 백신 후보가 미국에서 임상 시험을 거쳤습니다.
Pfizer Inc. — 백신 후보 BNT162b2
효능 : 2020 년 11 월, 3 상 시험의 초기 데이터는 Pfizer와 BioNTech에서 개발 한 mRNA 벡터 백신이 COVID-19 예방에 90 % 효과적 일 수 있음을 시사했습니다. 백신은 3 주 간격으로 2 회 연속 투여됩니다. 2 차 투여 7 일 후 감염률을 살펴보면 43,538 명 (30 %는 유색 인종)으로 구성된 연구 집단에서 94 명이 증상이있는 COVID-19에 걸렸습니다. 이로 인해 백신의 효능이 90 % 이상이되었습니다. 그들은 9 일 뒤인 11 월 18 일에 추가 데이터를 발표했는데, 시험 참가자들에게서 증상이있는 COVID-19가 170 건, 백신을 맞은 사람들이 8 건, 위약을받은 사람들이 162 건이 발생했다고 언급했습니다. 이로 인해 데이터가 개선되어 전체적으로 95 %의 효능 비율이 나타 났고 65 세 이상의 사람들에게는 94 %의 효능 비율이 나타났습니다. 이 데이터를 검토 한 후 FDA는 12 월에 첫 번째 투여 후 10 ~ 14 일 이내에 백신 접종을받은 연구 참가자의 감염률 감소를 언급 한 브리핑을 발표했습니다. 이스라엘에서 거의 600,00 명을 대상으로 대량 예방 접종을 한 결과 화이자 임상 시험에서와 유사한 효능 결과가 나타났습니다. 두 번째 투여 후, COVID-19에 대해 전체적으로 92 %의 효과가있는 것으로 나타났습니다. 증상이있는 질환에 대해 94 %, 무증상 질환에 대해 90 %입니다. 영국의 사전 인쇄 사례 관리 연구에서도 실제 세계에서 백신 접종의 효과를 조사했습니다. 70 세 이상의 노인 약 157,000 명을 살펴보면, 단일 백신은 14 일에 37 %, 21 일에 55 %, 28 일에 61 %, 그리고 35 일에 57 %의 비율로 증상 성 질환에 효과적이었습니다. 정량. 두 번째 투여 후 효과는 85 ~ 90 %로 증가했습니다. 첫 번째 투여 후 증상이있는 COVID-19가 발생한 사람들은 진단 후 14 일 이내에 입원해야 할 가능성이 43 % 더 적었고 감염으로 사망 할 가능성이 51 % 더 낮았습니다.
바이러스 변종
변종이라고도 알려진 바이러스의 일부 균주는 스파이크 단백질에서 일부 백신의 효과를 변경할 수있는 돌연변이를 개발했습니다. 지금까지 많은 변종이 발견되었습니다. 여기에 가장 많이 연구 된 세 가지가 있습니다.
- 영국 변종 : B.1.1.7 또는 20I / 501Y.V1로도 알려진이 변종은 17 개의 돌연변이 (스파이크 단백질에서 8 개)를 포함하며 2020 년 9 월에 처음 발견되었습니다.
- 남아프리카 변종 : B.1.351 또는 20H / 501Y.V2로도 알려진이 변종은 21 개의 돌연변이 (스파이크 단백질에서 10 개)를 포함하며 2020 년 10 월에 처음 발견되었습니다.
- 브라질 변종 : B.1.28.1 또는 20J / 501Y.V3라고도하는이 변종은 17 개의 돌연변이 (스파이크 단백질에있는 3 개)를 포함하며 2021 년 1 월에 처음 발견되었습니다.
바이러스 변종 : 화이자는 21 일 간격으로 두 백신을 모두 접종받은 40 명의 혈청을 평가하고 중국 우한에서 검출 된 원래 바이러스와 유사한 바이러스 (대조군으로)와 스파이크가있는 바이러스에 대해 테스트했습니다. 영국 변종에서 발견되는 단백질 돌연변이. 목표는 혈청이 이러한 바이러스를 중화시키는 데 얼마나 효과적인지 확인하는 것이 었습니다. 젊은 연구 참가자 (23-55 세, n = 26)의 혈청은 78 % 비율로 영국 변이체를 중화 시켰고, 나이가 많은 참가자 (57-73 세, n = 14)의 혈청은 83 % 비율로 중화되었습니다. 그런 다음 다른 변종에 대해 테스트를 계속했습니다. 중화 항체 분석은 대조군 바이러스, 영국 및 남아프리카 변종을 나타내는 N501Y 돌연변이, 영국 변종을 나타내는 69 / 70- 결실 + N501Y + D614G 돌연변이를 갖는 바이러스를 사용하여 백신 접종 된 20 명의 혈청에 대해 수행되었습니다. 남아프리카 변종을 나타내는 E484K + N501Y + D614G 돌연변이를 가진 바이러스. 혈청 중 6 개에서 역가는 남아프리카 변종에 비해 절반에 불과했습니다. 즉, 혈청 중 10 개에서 역가는 영국 변종에 비해 두 배나 높았습니다. 전체적으로 백신은 대조군과 비교할 때 0.81 배에서 1.46 배 범위의 차이로 이러한 변종에 대해 효과적인 상태를 유지했습니다. 15 명의 예방 접종을받은 수혜자의 혈청 예비 보고서뉴 잉글랜드 의학 저널B.1.351 변종을 무력화하는 능력이 3 분의 2 감소 함을 발견했습니다. 화이자는 COVID-19 변종에 대한 항체 반응을 높이는 방법으로 세 번째 백신 접종을 검토하고 있습니다.
어린이 : 화이자는 어린이에게 백신의 효과를 조사하고 있습니다. 그들의 3 상 시험에는 현재 12 ~ 15 세 어린이 2,200 명 이상과 16 ~ 17 세 청소년 750 명 이상이 포함됩니다.
보관 : 콜드 체인 기술을 사용하여 백신을 보관해야한다는 우려가 제기되었습니다. 즉, 섭씨 -70도 (화씨 -94도)에서 동결시키는 것입니다. 화이자는 GPS 열 추적 기능이있는 드라이 아이스를 사용하는 특수 온도 제어 용기를 개발하여 배송 중에 백신이 적절한 온도로 유지되도록했습니다. FDA에 제공된 데이터에 따르면 백신은 최대 2 주까지 표준 냉동고 온도에서 안정적으로 유지됩니다. 이렇게하면 더 많은 사이트에서 백신에 접근 할 수있게 될 것입니다.
승인 :이 백신은 12 월 2 일 영국에서 사용이 승인되었습니다. 12 월 8 일, 영국에서 온 90 세의 마가렛 키넌은 세계에서 처음으로 백신을 접종받은 비 연구 참가자였습니다. 12 월 11 일 FDA는 미국에서 응급 사용 허가를 받았고 12 월 14 일 첫 미국인이 예방 접종을 받았습니다.
논란 : COVID-19의 확산이 증가함에 따라 영국은 권장되는 3 주가 아닌 12 주 간격으로 백신을 투여 할 계획을 발표했습니다. 이것이 백신의 첫 번째 접종을받는 사람의 수를 증가시킬 것이지만, 화이자와 BioNTech는 그들의 임상 시험에 그러한 투여 일정의 효과를 뒷받침 할 데이터가 없다고 밝혔습니다. 현재 미국은 권장되는 3 주 투여 일정을 계속할 것입니다.
Moderna Inc. — 백신 후보 mRNA-1273
예비 결과 : NIAID (National Institute of Allergy and Infectious Diseases)와 BARDA (Biomedical Advanced Research and Development Authority)의 자금 지원을 받아 Moderna는 1 단계 백신 시험의 예비 결과를 발표했습니다.뉴 잉글랜드 의학 저널4 주 간격으로 mRNA 백신을 2 회 투여 한 후 45 명의 연구 참가자가 회복기 혈장에서 보이는 것과 비슷한 농도의 중화 항체를 개발했습니다. 후속 2 상 시험은 원숭이에서 유망한 결과를 보여주었습니다. 24 마리의 히말라야 원숭이를 백신이나 위약으로 치료하고 4 주 간격으로 두 번의 주사를 맞았습니다. 그런 다음 그들은 고용량의 COVID-19에 직접 노출되었습니다. 2 일 후, 백신 접종 된 원숭이 중 8 명 중 1 명만이 바이러스가 검출되었고 위약으로 치료받은 모든 원숭이가 감염되었습니다. 다시 말하지만, 중화 활성은 회복기 혈청에서 보인 것보다 상당히 높았습니다. 그들은 또한 스파이크 단백질에 대한 CD4 T 세포 반응을 감지했습니다.
효능 : 2020 년 11 월 3 상 시험 데이터에 따르면 Moderna 백신은 COVID-10에 대해 94.5 %입니다. 두 번째 투여 2 주 후 감염률을 살펴보면 65 세 이상 7,000 명 이상과 유색 인종 11,000 명 이상을 포함한 30,000 명 이상의 연구 집단에서 95 명이 증상이있는 COVID-19에 걸렸습니다.인구의 42 %는 당뇨병, 심장병 또는 비만과 같은 고위험 상태를 가졌습니다. 이 질병에 걸린 사람 중 11 건은 중증으로 분류되었지만 백신을 맞은 사람은 없었습니다. 12 월에 그들은 추가 데이터를 발표했는데, 임상 시험 참가자들에게서 196 건의 증상 감염 사례가 발생했으며, 백신을 맞은 사람 (중증 COVID-19는 없었 음) 11 건, 위약을 복용 한 사람 185 건이 있었다. 이는 COVID-19에 대해 크게 94.1 %, 중증 질환에 대해 100 % 효능을 시사했습니다. 데이터에 대한 동료 검토가 보류 중입니다.
바이러스 변종 : Moderna는 B.1.1.7 및 B.1.351 변종에 대한 1 상 시험에서 백신을 접종 한 8 명의 혈청을 테스트하는 시험관 내 분석을 수행했습니다. 이 회사는 영국 변종에 비해 중화 역가가 크게 감소하지 않았지만 남아프리카 변종에 비해 역가가 6 배 감소했다고 주장했습니다. 이러한 이유로 그들은 B.1.351 변종을 표적으로하기 위해 추가 용량을 조사하고 개발하고 있습니다. 예방 접종 된 수혜자의 혈청에 대한 예비 보고서뉴 잉글랜드 의학 저널B.1.17 변종을 중화하는 능력은 1.2 배 감소했지만 B.1.351 변종에 비해 6.4 배 감소했습니다.
어린이 : Moderna는 12 세 미만의 어린이를위한 시험을 진행하고 있습니다.
면역 기간 : 중요하게도 Moderna는 백신 반응의 예상 기간에 대한 데이터를 발표했습니다. 1 상 시험은 28 일 간격으로 2 회 접종을받은 34 명의 사람들을 평가하고 그들의 항체 반응을 COVID-19에서 회복 된 41 명의 대조군과 비교했습니다. 연구원들은 중화 항체가 두 번째 백신 접종 후 90 일 동안 실제로 질병에 걸린 사람들보다 더 높은 농도로 지속된다는 것을 발견했습니다. 이것은 백신이 합리적인 기간의 면역을 제공 할 수 있기를 희망합니다. 면역 반응의 실제 기간을 결정하려면 더 많은 장기 데이터가 필요합니다.
보관 : 콜드 체인 기술이 필요한 화이자 백신과 달리 Moderna 백신은 섭씨 영하 4도 (화씨 -20도)의 표준 냉동고에서 6 개월 동안, 일반 냉장고 온도는 30 일 동안, 실온에서는 12 시간 동안 보관할 수 있습니다.
승인 : FDA는 2020 년 12 월 18 일에 Moderna 백신 긴급 사용 허가를 승인했습니다. 첫 번째 접종은 12 월 21 일에 투여되었습니다. 영국은이 백신의 사용을 2021 년 1 월 8 일에 승인했습니다.
논란 : FDA는 이용 가능한 공급량과 첫 번째 접종으로 예방 접종을받을 수있는 사람의 수를 늘리기 위해 Moderna 백신의 복용량을 줄이는 것을 고려하고 있습니다. 2 상 시험 데이터에 따르면 백신의 절반 용량은 55 세 이하의 사람들에게 전체 용량과 동일한 수준의 면역을 제공했습니다. 그러나이 데이터에는 수백 명의 사람들이 포함되었으며 백신에 대한 면역 반응이 있었는지, 즉 항체가 발생했는지를 결정하기위한 실험에서 나왔습니다. 3 상 시험은 실제로 COVID-19에 대한 효과를 평가 한 것입니다. 후자의 연구에서는 전체 백신 용량이 사용되었습니다.
AstraZeneca — 백신 후보 AZD1222 (이전 : ChAdOx1)
예비 결과 : AstraZeneca와 협력하여 Oxford University의 Jenner Institute는 백신 연구 분야에서 앞서 가고 있습니다. 다른 유형의 코로나 바이러스에 대한 백신이 작년에 소규모 인간 실험에서 가능성을 보여 주었기 때문에 Jenner Institute는 빠르게 전진 할 수있었습니다. 아데노 바이러스 벡터 백신을 처음 주사 한 후, 백신을 접종 한 35 명의 연구 참가자 중 91 %에서 중화 항체가 발생하여 28 일에 최고치를 기록했으며 56 일 동안 높은 수준을 유지했습니다. 4 주에 추가 백신을 접종 한 모든 참가자에게서 중화 항체가 발견되었습니다. 그들의 백신은 또한 7 일 후에 기록 된 T 세포 반응을 보였고, 14 일에 최고점에 이르렀고, 최대 56 일까지 지속되었습니다. 일시적으로 백신참가자가 바이러스에 의해 유발 될 수있는 신경 학적 질환 인 횡 척수염이 발생한 후 2020 년 9 월에 임상 3 상 시험을 중단했습니다. 이 질병이 백신과 관련이 없다는 것을 확인한 후 AstraZeneca는 6 주 후에 시험을 재개했습니다. 11 월에 더 많은 동료 검토 단계 II / III 데이터가 발표되었습니다. 560 명의 연구 참여자가 증가함에 따라 99 %의 사람들이 추가 접종 후 2 주 이내에 중화 항체를 개발했습니다.
효능 : 12 월에 AstraZeneca는 두 가지 다른 연구 시험에서 11,000 명 이상의 연구 참가자에 대한 동료 검토 데이터를 발표했습니다. 백신 효능 률은 2 개의 전체 용량 백신을 한 달 간격으로 투여 한 후 62 % (n = 8,895) 였고, 절반 용량을 투여 한 후 한 달 후 전체 용량을 투여했을 때 (n = 2,741) 90 %였습니다. 70.4 %. 2 월에 그들은 더 많은 3 단계 데이터를 발표했는데, 이번에는 17,100 명이 넘는 참가자의 더 많은 인구에 대한 데이터입니다. 단일 투여 후 효능은 22 ~ 90 일 후에 76 %로 나타났습니다 (전체 투여 그룹의 경우 59 %, 절반 투여 그룹의 경우 86 %). 2 회 투약 후 14 일 후의 효능은 증상이있는 COVID-19에 대해 67 %였습니다 (전체 용량 그룹의 경우 57 %, 절반 용량 그룹의 경우 74 %). 흥미롭게도 효능은 투여시기의 영향을 받았습니다. 6 주 미만 간격으로 투여했을 때는 55 % (전체 용량 그룹의 경우 33 %, 절반 용량 그룹의 경우 67 %)로 낮았지만 용량을 12 주 이상 분리했을 때는 82 %로 증가했습니다 (63 전체 용량 그룹의 경우 %, 절반 용량 그룹의 경우 92 %). 참고로이 효능은 COVID-19로 인한 증상이있는 사람을 기반으로하며 무증상 COVID-19 감염을 반영하지 않습니다. 영국의 사전 인쇄 사례 대조 연구에서는 70 세 이상의 사람들을 대상으로 한 단일 접종의 효과를 조사했습니다. 연구자들은 실제 세계에서 COVID-19 검사를받은 약 157,000 명의 사람들을 조사했습니다. 증상 성 질환에 대한 백신 효과는 14 일에 22 %, 21 일에 45 %, 28 일에 60 %, 35 일에 73 %였습니다. 백신 접종에도 불구하고 증상이있는 COVID-19가 발생한 사람들은 진단 후 14 일 이내에 입원해야 할 가능성이 37 % 낮았습니다.
바이러스 변종 : B.1.1.7 변종에 대한 효능을 확인하기 위해 연구자들은 COVID-19에 감염된 499 명의 II / III 상 참가자로부터 바이러스 게놈을 시퀀싱했습니다. 원래 바이러스에 비해 B.1.1.7에 대한 중화 항체가 9 배 감소했습니다. B.1.1.7 변종에 노출 된 사람들의 경우, 증상이있는 COVID-19 감염에 대한 효능은 75 % 였지만 무증상 감염에 대해서는 27 %에 불과했습니다. 이는 원래 균주의 경우 각각 84 % 및 75 %와 대조됩니다. 안타깝게도 남아공에서는 B.1.351로 인한 경증에서 중등도 COVID-19에 대해 효과가 없다는 데이터가 나타난 후 백신 투여가 중단되었습니다.
보관 : mRNA 백신과 달리 백신은 냉동 할 필요가 없으며 일반 냉장 온도에서 보관할 수 있습니다.
승인 :이 백신은 2020 년 12 월 30 일 영국에서 사용하도록 승인되었습니다. 첫 번째 접종은 2021 년 1 월 4 일에 시행되었습니다. 세계 보건기구는 2020 년 2 월에 백신 사용을 권장했습니다.
논란 : 영국은 화이자 백신과 유사하게 AstraZeneca 백신의 투여 일정을 4 주에서 12 주로 변경한다고 발표했습니다. 사용 가능한 데이터에 따르면 전체 용량의 백신을 투여받은 사람들에게이 빈도로 투여했을 때 유사한 효능이 있음을 시사합니다.
Johnson & Johnson — 백신 후보 Ad26.COV2.S
예비 결과 :이 백신은 Johnson과 Johnson의 사업부 인 Janssen Pharmaceutical Companies에서 개발 중입니다. SARS-CoV-2가 발현하는 스파이크 단백질을 공격하는 아데노 바이러스 벡터 백신입니다. 52 명의 붉은 털 원숭이 원숭이를 대상으로 한 연구에 따르면 한 번의 주사로 바이러스에 대한 보호와 함께 항체 반응을 중화시키는 것으로 나타났습니다. 56 명의 성인을 대상으로 1 회 또는 2 회 투여 일정을 사용하여 안전성을 평가 한 I / II 상 시험. 1 회 투여 후 혈청 전환 (스파이크 단백질에 대한 항체 발생)은 99 % 였고 스파이크 단백질에 대한 T 세포 반응은 83 %에 도달했습니다. 이 백신은 연속 2 회 접종이 아닌 1 회 접종을 필요로하는 유일한 현재 후보이기 때문에 가능성을 보여줍니다. 2020 년 10 월 Johnson & Johnson은 연구 참가자 중 한 명에게 설명 할 수없는 질병을보고했습니다. 회사는 질병이 백신과 관련이 없다는 것이 확인 될 때까지 11 일 동안 임상 시험을 중단했습니다. 그 이후로 더 많은 I / II 상 데이터가 발표되어 18 ~ 55 세와 65 세 이상의 두 연령 그룹에서 중화 항체 반응을 보여줍니다. 그들은 또한 상이한 투여 요법, 예를 들어 고용량 대 저용량 및 단일 용량 대 2 회 용량을 56 일 간격으로 비교했다. 총 805 명의 참가자가 예방 접종을 받았습니다. 29 일까지 평균 90 %의 사람들이 중화 항체를 가졌습니다 (투약 요법에 따라 젊은 코호트의 경우 92-99 %, 노인 코호트의 경우 88-96 %). 57 일째에 혈청 전환율은 연령이나 투여 요법에 관계없이 모든 사람에게 100 %였습니다.
효능 : 3 상 임상 시험에는 43,000 명 이상의 사람들이 포함되었으며 468 건의 COVID-19 증상이있었습니다. 이 백신은 중증 감염에 가장 효과적이었으며 28 일 후에 85 %의 효과를 보였으며 49 일 이후에는 사례가 발견되지 않았습니다. 전체 효과는 66 % (미국 72 %, 라틴 아메리카 66 %, 남아프리카 57 %)였습니다. ). 참고로 남아공 사례의 95 %는 B.1.351 변종에서 발생했습니다.
승인 : Johnson & Johnson 백신은 2021 년 2 월 27 일 1 회 접종으로 FDA 긴급 사용 승인을 받았습니다. WHO는 2021 년 3 월 12 일에 승인을 받았습니다.
Novavax Inc. — 백신 후보 NVX-CoV2373
예비 결과 : NIAID (National Institute of Allergy and Infectious Diseases)와 BARDA (Biomedical Advanced Research and Development Authority)가 후원하는이 백신은 스파이크 단백질에 대한 항체 반응을 개발하기 위해 나노 입자 기술을 사용합니다. 다른 많은 백신과 마찬가지로 21 일 간격으로 2 회 투여됩니다. I / II 상 임상 시험에서 COVID-19 증상이있는 환자의 회복기 혈장에서 보이는 것보다 더 큰 항체 반응이 나타났습니다. 임상 3 상 시험은 30,000 명의 연구 참가자를 목표로 적극적으로 등록하고 있으며, 그중 3 분의 2는 백신, 나머지는 위약을 받게됩니다.
효능 : 보도 자료에서 회사는 영국에서의 3 상 시험 (참가자 15,000 명 이상)과 남아프리카에서의 2 상 시험 (참가자 4,400 명 이상)의 예비 결과를 발표했습니다. 이전 연구에서 62 명의 참가자가 증상이있는 COVID-19에 걸렸습니다 (치료군 6 명 vs 위약군 56 명). 전체적으로 백신의 효과는 89.3 %였습니다. 이것은 원래 변종에 대해 95.6 %, 영국 변종에 대해 85.6 %로 나뉩니다. 후자의 연구는 전체 효과가 60 % 인 증상이있는 COVID-19 44 건 (치료군 15 건 대 위약군 29 건)의 경우 덜 성공적이었습니다. 시퀀싱은 양성 사례 중 27 개에서만 수행되었지만 그중 25 개는 남아프리카 변종으로 확인되었습니다.
INOVIO Pharmaceuticals Inc. — 백신 후보 INO-4800
전염병 대비 혁신 연합 (Coalition for Epidemic Preparedness Innovations)과 빌 앤 멜린다 게이츠 재단 (Bill and Melinda Gates Foundation)은이 백신 후보에 대한 여러 자금 출처 중 하나입니다. INOVIO Pharmaceuticals, Inc.에서 개발 한이 DNA 백신의 첫 번째 주사는 2020 년 4 월 6 일에 건강한 피험자에게 투여되었습니다. 2020 년 9 월 FDA는 전달 장치의 안전성을 평가하면서 II / III 상 임상 시험을 보류했습니다. 이 회사는 2021 년 2 분기에 임상 시험을 재개 할 예정입니다.
생물학적 제제
COVID-19의 심각한 사례는 사이토 카인 폭풍이라고하는 것과 관련이 있습니다. 정상적인 면역 반응의 일부로 신체는 면역계 세포에서 분비되는 단백질 인 사이토 카인을 감염 부위로 모집합니다. 그러나 어떤 경우에는 그 과정이 과민 반응을 일으키고 과도한 사이토 카인이 방출됩니다. 이러한 사이토 카인 중 일부는 본질적으로 염증성이며 호흡기 증상의 악화 또는 장기 부전으로 이어질 수 있습니다. 이 문제를 해결하기 위해 생물학적 제제 (생물학적 출처에서 생성 된 약물 치료)가 현재 고려되고 있습니다.
바리 시티 닙
바리 시티 닙은 JAK1 / JAK2 억제제로, 특정 사이토 카인의 효과를 감소시켜 염증에 사용되는 약물입니다.
연구 결과 : 적응 형 COVID-19 치료 시험 (ACTT-2)의 일환으로 3 상 무작위 이중 맹검 위약 대조 시험에서 약물에 대한 조기 가능성을 보여주었습니다. COVID-19로 입원 한 약 1,000 명의 환자가 무작위 배정되어 렘 데시 비르 단독 또는 바리 시티 닙과 함께 렘 데시 비르를 투여 받았습니다. 평균적으로 환자들은 병용 치료로 하루 전에 임상 적으로 개선되었습니다. 2020 년 11 월 FDA는 산소 보충, 인공 호흡기 치료 또는 체외 막 산소 공급 (ECMO)이 필요한 입원 환자 치료를위한 응급 사용 승인을 위해 약물 조합 (바리 시티 닙 단독이 아님)을 승인했습니다. 그러나 국립 보건원은 덱사메타손을 사용할 수있을 때이 요법을 선호하는 치료법으로 뒷받침 할 충분한 증거가 없다고 밝혔습니다.
인터페론 베타 -1a
인터페론은 면역 체계의 자연스러운 부분입니다. 이 사이토 카인은 바이러스에 대한 면역 반응을 향상시킵니다. 현재 인터페론은 현재 바이러스 성 간염에 사용되는 주사 치료제입니다.
연구 결과 : COVID-19는 대부분의 경우 폐 질환이기 때문에 연구원들은 인터페론 베타 -1a를 폐로 호흡하는 것이 바이러스에 대한 면역 반응을 높이는 데 도움이 될 수 있는지 확인했습니다. 임상 2 상 무작위 이중 맹검 임상 시험랜싯 호흡기 의학COVID-19로 입원 한 성인 약 100 명을 조사했습니다. 참가자들은 분무기 또는 위약을 통해 14 일 동안 흡입 된 인터페론 베타 -1a로 치료 받았습니다. 인터페론 그룹은 15 ~ 16 일 후 임상 적 개선이 2 배, 28 일에 3 배 개선되었습니다. 입원 기간은 줄어들지 않았지만 질병 또는 사망의 심각성은 79 % 감소했습니다.
토 실리 주맙
토 실리 주맙은 전 염증성 사이토 카인 중 하나 인 인터루킨 -6 (IL-6)에 대한 세포 수용체의 결합을 차단하는 단일 클론 항체입니다. 이것은 이론적으로 사이토 카인 폭풍의 심각성을 감소시키고 사람들이 더 빨리 회복하는 데 도움이 될 것입니다.
연구 결과 :
연구바소 류마티스 학토 실리 주맙으로 치료받은 COVID-19 폐렴 환자의 인공 호흡기 사용 또는 사망 위험이 표준 요법으로 치료받은 환자에 비해 39 % 감소한 것으로 나타났습니다. 그러나 토 실리 주맙은 면역 억제제 역할을하며 연구자들은 또한이 약물로 치료받은 사람들이 침습성 아스 페르 길 루스 증과 같은 다른 새로운 감염 발병률이 3 배 증가한다는 것을 발견했습니다. 154 명의 환자를 대상으로 한 연구에 따르면임상 전염병, 토 실리 주맙은 인공 호흡기가 필요한 COVID-19 환자의 사망률을 약물로 치료하지 않은 환자에 비해 45 % 감소 시켰습니다. 토실 루주 맙으로 치료받은 사람들은 47 일의 후속 조치 동안 과감 염이 발생할 가능성이 더 높았지만 (54 % 대 26 %), 이러한 과감 염의 결과로 사망이 증가하지는 않았습니다.
세 가지 연구가 발표되었습니다.JAMA 내과2020 년 10 월에 결과가 일치하지 않았습니다. 미국 연구에 따르면 중환자 실에 입원 한 지 2 일 이내에 중증 COVID-19 환자 433 명을 치료했습니다. 그들의 사망률은 토 실리 주맙을 투여받지 않은 ICU 환자의 41 %에 비해 29 %였습니다. 그러나 프랑스와 이탈리아 연구는 COVID-19 폐렴 환자를위한 무작위 공개 시험에서 임상 적 이점을 찾지 못했습니다. 전자의 연구는 중등도에서 중증의 질병을 가진 130 명과 126 명을 대상으로했습니다. 28 일째 사망률이나 14 일째 치료를 통한 증상 호전에는 차이가 없었다. 다른 연구뉴 잉글랜드 의학 저널COVID-19 폐렴을 앓고있는 거의 400 명의 사람들을 조사했습니다. 토 실리 주맙으로 치료받은 사람들은 28 일까지 기계적 인공 호흡이 필요할 가능성이 적었습니다 (표준 치료와 비교했을 때 12 % 대 19 %). 임상 결과는 개선되었지만 사망률은 크게 변하지 않았습니다.
불행히도 모든 연구가 이점을 보여준 것은 아닙니다. 일부는 잠재적 인 해를 입었습니다. 129 명의 중환자 COVID-19 환자를 대상으로 한 브라질 연구에서 표준 치료 또는 표준 치료만으로 토 실리 주맙 치료를 받았습니다. 15 일째에 토 실리 주맙으로 치료받은 사람들의 사망률은 17 % 대 3 %였습니다. 29 일째에 사망률은 두 그룹간에 통계적으로 유의하지 않았습니다. 다른 연구에서 생존 혜택이 나타 났지만이 연구는 안전성에 대한 중요한 문제를 제기합니다. 사실이 연구는 이러한 이유로 조기 종료되었습니다.
국립 보건원은 현재 기계적 환기 또는 고 유량 비강 캐뉼라 산소가 필요한 ICU의 COVID-19 환자에게 토 실리 주맙과 덱사메타손을 권장합니다. 저산소증이 발생하고 비 침습적 인공 호흡이나 고 유량 산소가 필요한 비 ICU 환자도 염증 마커가 높으면이 요법을받을 수 있습니다. 즉, 토 실리 주맙은 면역력이 현저히 저하 된 사람에게는 사용해서는 안됩니다.
기타 항 바이러스제
현재 COVID-19에 대해 조사중인 여러 항 바이러스 치료법 (바이러스의 번식 능력을 막는 약물)이 있습니다.
몰누 피라 비르
Molnupiravir는 일부 RNA 바이러스의 복제를 차단하는 약물입니다. 이것은 신체에서 활성 형태 (N4- 하이드 록시 시티 딘)로 대사되는 비활성 약물 인 전구 약물입니다. 이 약물은 Merck와 Ridgeback Biotherapeutics에 의해 개발되었습니다.
연구 결과 : 2 상 임상 시험에는 COVID-19 증상이있는 입원하지 않은 사람 78 명이 포함되었으며 기준선 비 인두 면봉에서 바이러스 수준이 검출되었습니다. molnupiravir를 사용한 치료는 5 일 (0/47)까지 바이러스 부하를 0으로 줄 였지만 위약 그룹의 24 % (6/25)에서 바이러스가 검출 가능한 상태를 유지했습니다. 치료로 인한 심각한 부작용은 없었습니다.
인플루엔자 약물
Favipiravir와 arbidol은 인플루엔자를 치료하는 데 사용되는 항 바이러스 약물입니다. 고농도에서는 COVID-19에 효과적 일 수 있습니다.
연구 결과 : 240 명의 COVID-19 환자를 대상으로 한 연구에서 연구원들은 파비 피라 비르 효과를 아르 비돌과 비교했습니다. 기침과 발열의 증상은 arbidol보다 favipiravir가 훨씬 빨리 호전되었지만 회복률에는 7 일째 큰 차이가 없었습니다. 두 약물 모두 경미한 부작용으로 잘 견디 었습니다.
로 피나 비르-리토 나비 르
Lopinavir-ritonavir는 COVID-19에 효과적 일 수있는 HIV 치료에 사용되는 한 쌍의 항 바이러스 약물입니다.
연구 결과 : COVID-19로 인한 폐렴 및 산소 수치가 낮은 199 명을 대상으로 한 연구에서 94 명에게로 피나 비르-리토 나비 르를 투여하고 나머지는 위약을 투여했습니다. 로 피나 비르-리토 나비 르로 치료받은 더 많은 사람들이 14 일째까지 증상이 호전되었지만 (45.5 % 대 30 %) 산소 요법 기간, 기계적 환기의 필요성에 관해서는 두 그룹간에 큰 차이가 없었습니다. 입원 기간 또는 사망률. 또 다른 연구에서는 COVID-19로 입원 한 성인 127 명을로 피나 비르-리토 나비 르, 리바비린 및 인터페론 β-1b를 사용한 삼중 요법 또는로 피나 비르-리토 나비 르 단독 요법으로 무작위 배정했습니다. 3 중 치료군의 환자는 바이러스 배출을 더 일찍 중단하고 (7 일 vs. 12 일), 증상이 더 일찍 개선되었고 (4 일 vs. 8 일), 더 일찍 퇴원했습니다 (9 일 vs. 15 일).
하이드 록시 클로로퀸 및 클로로퀸
Hydroxychloroquine과 chloroquine은 말라리아 및 루푸스 및 류마티스 관절염과 같은자가 면역 질환을 치료하기 위해 현재 FDA 승인을받은 약물입니다.단백질 글리코 실화 및 기타 효소 과정을 방해함으로써 이러한 약물은 COVID-19가 인간 세포에 결합, 진입 및 복제되는 것을 방지 할 수 있다고 믿어집니다.
hydroxychloroquine과 chloroquine을 비교 한 연구는 hydroxychloroquine이 약간 덜 강력하지만 시험관 내에서 COVID-19에 대해 잠재적으로 효과적이라는 것을 발견했습니다.
연구 결과
프랑스의 한 연구가 hydroxychloroquine과 chloroquine 연구를 주도했습니다. 처음에는 hydroxychloroquine 요법으로 치료받은 26 명의 COVID-19 환자와 치료되지 않은 16 명의 대조군 환자가 포함되었습니다. 히드 록시 클로로퀸으로 치료받은 환자 중 6 명은 아지트로 마이신 (여러 감염에 대해 처방되는 Z-Pack이라고도 함)으로도 치료를 받았습니다. 서류상 결과는 유망 해 보였습니다. 6 일째에 연구 저자는 하이드 록시 클로로퀸으로 치료받은 사람들이 바이러스 부하 (혈액 내 바이러스 양)를 57 % 줄였으며 아지트로 마이신 치료를받은 사람들도 바이러스를 완전히 제거했다고 지적했습니다.
이것이 고무적이기는했지만,이 연구는 환자가 임상 적으로 어떻게 지 냈는지, 즉 증상이 호전되기 시작했는지 여부에 대해서는 다루지 않았습니다. 또한 치료로 인해 연구 참여자가 연구원과 후속 조치를 취하지 못하는 의학적 문제가 발생했는지 여부 (1 명 사망, 3 명 중환자 실로 이송, 1 명은 약물 부작용으로 치료 중단, 1 명은 퇴원)가 불분명했습니다.
FDA는 지난 3 월 COVID-19에 대한 클로로퀸 포스페이트와 하이드 록시 클로로퀸 설페이트 제품에 대한 비상 사용 허가를 6 월 15 일에 승인했지만, 비효율 성과 심각한 부작용을 이유로 허가를 취소했습니다.
이러한 약물의 사용을 뒷받침하는 일화적인 증거가 있지만 후속 연구에서는 동일한 이점을 보여주지 못했습니다. 두 번째 프랑스 연구는 원래 연구와 동일한 프로토콜을 따랐지만 hydroxychloroquine이 증상을 크게 개선하거나 신체에서 바이러스 제거를 감소시키지 않는다는 것을 발견했습니다. 다른 여러 연구에서 COVID-19에 걸린 사람들을 치료할 때 하이드 록시 클로로퀸이 위약보다 더 효과적이지 않음을 보여주었습니다. 2020 년 9 월, 이중 맹검 위약 대조 무작위 임상 시험JAMA 내과하이드 록시 클로로퀸은 132 명의 의료 종사자의 감염 예방에 효과가 없다고 결론지었습니다. 류마티스 질환을 치료하기 위해 정기적으로 하이드 록시 클로로퀸을 복용하는 사람들도 마찬가지입니다. 또 다른 연구에 따르면 하이드 록시 클로로퀸을 복용해도 약물을 복용하지 않는 사람들과 비교할 때 COVID-19에 걸릴 위험이 감소하지 않았습니다.
더 우려되는 것은 이러한 약물의 잠재적 인 부작용입니다. 브라질 연구는 다량의 클로로퀸으로 인한 합병증으로 인해 조기에 중단되어야했습니다. ㅏJAMA연구에 따르면 hydroxychloroquine 치료는 COVID-19 환자의 20 % 이상에서 QT 간격을 연장 시켰으며 이는 생명을 위협하는 심장 부정맥의 발생과 관련 될 수있는 심전도 (ECG)에서 발견되었습니다.
모든 보고서가 나쁜 것은 아닙니다. COVID-19 치료에서 하이드 록시 클로로퀸의 잠재적 인 이점을 보여주는 연구가 발표되었습니다. 연구원들은 2,500 명 이상의 성인을 연구 한 결과, 약물 치료를받지 않은 사람은 26 %에 비해 14 %의 사망률을 보였습니다. hydroxychloroquine과 azithromycin을 결합했을 때 사망률은 20 %였다. 그러나 스테로이드 덱사메타손으로 치료받은 사람들의 수가 치료군에서 상당히 많았 기 때문에이 연구에 대한 논란이 있으며, 이는 히드 록시 클로로퀸이나 아지트로 마이신이 아닌 스테로이드에서 얻을 수 있음을 시사합니다. 모든 연구 참가자의 68 %가 스테로이드로 치료를 받았지만, 비 치료 그룹의 35 %만이 덱사메타손을 투여 받았습니다. 하이드 록시 클로로퀸 그룹의 약 79 %와 아지트로 마이신 그룹과 결합 된 하이드 록시 클로로퀸 그룹의 74 %도 스테로이드를 투여 받았습니다.
Verywell의 한마디
불확실한이시기에 희망을 제공하는 것도 중요하지만, 우리 자신을 보호 할 객관적이고 과학적으로 입증 된 방법을 찾는 것도 중요합니다. 수백 건의 임상 실험이 진행 중이기 때문에 무엇이 효과가 있고 무엇이 효과가 없는지에 대해 경계해야합니다. 치료는 인구의 많은 부분을 치료하는 데 사용하기 전에 안전하고 효과적인 것으로 입증되어야합니다.