Sasiistock / 게티 이미지
핵심 사항
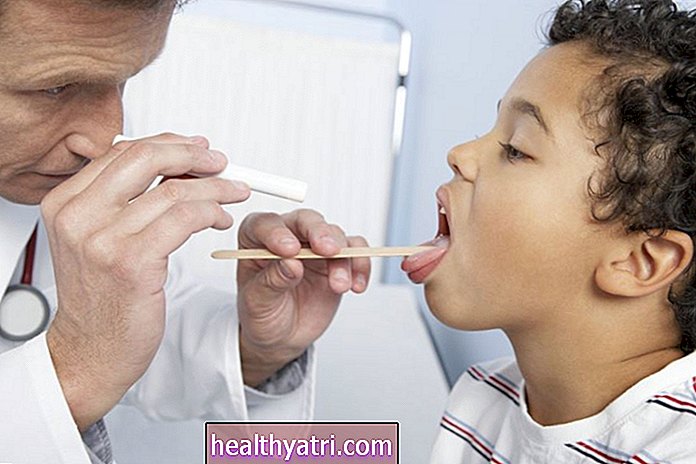
- 화이자는 12 세 이상의 어린이를 대상으로 코로나 바이러스 백신 테스트를 시작하기 위해 FDA 승인을 받았습니다.
- 전문가들은 임상 시험에 어린이를 포함시키는 것이 COVID-19로부터 어린이와 성인 모두를 보호 할 백신의 전반적인 개발에 중요하다고 말합니다.
- 웹 사이트에 따르면 Pfizer는 이미 39,000 명 이상의 자원 봉사자를 연구에 등록했습니다. 자원 봉사자 중 34,000 명 이상이 이미 두 번째 예방 접종을 받았습니다.
미국 제약 회사 인 화이자는 지난 10 월 미국 식품의 약국 (FDA)으로부터 코로나 바이러스 백신 시험에 12 세 어린이를 등록하기 시작하는 허가를 받았다고 발표했습니다.
"그렇게함으로써 우리는 더 많은 연령과 배경을 가진 개인들에게 백신의 잠재적 인 안전성과 효능을 더 잘 이해할 수있을 것"이라고 회사는 업데이트 된 성명에서 밝혔다.
이것은 어린이를 포함하는 미국 최초의 COVID-19 백신 시험입니다. 10 월 현재 화이자는 3 상 임상 시험에서 백신을 보유한 미국 4 개 기업 중 하나입니다.
화이자는 이미 임상 3 상을 16 세 이상의 어린이와 만성 안정된 인체 면역 결핍 바이러스 (HIV), C 형 간염, B 형 간염 환자로 확대했습니다.
어린이에게 COVID-19 백신을 검사하는 이유는 무엇입니까?
화이자가 어린이 테스트 시작 승인을 받기 전에 전문가들은 저널에 보고서를 발표했습니다.임상 전염병이러한 테스트의 중요성을 설명합니다.
이 보고서는“코로나 19가 어린이에게 미치는 직접적인 영향은 현재 우리가 효과적인 소아 백신을 보유하고있는 다른 여러 병원체에서 관찰 된 것보다 큽니다. “또한, SARS-CoV-2 전파에서 어린이의 역할은 분명히 과소 평가되었습니다. 신중하게 수행 된 2 상 임상 시험은 잠재적 인 COVID-19 백신 안전 문제를 적절히 해결할 수 있습니다.”
수잔 팜, MD
아이들에게 예방 접종을하지 않으면이 바이러스의 확산을 극복 할 수 없습니다.
— 수잔 팜, MD뉴욕에있는 Stony Brook Children 's Hospital의 소아 감염증 부서장 인 Sharon Nachman MD는이 보고서에 동의하며 Verywell은 다음과 같이 말했습니다.“소아과 의사는 연구의 세부 사항을보고 백신이 어린이에게 어떻게 작용할 것인가에 매우 관심이 있습니다. .”
Nachman에 따르면 어린이에게 백신을 테스트하면 특별한 이점이 있습니다. 연구진은 성인에게 사용되는 백신이 어린이에게 필요한지 또는 더 낮은 용량에 대해 유사한 면역 반응을 보이는지 파악하는 것을 포함하여 단기 및 장기 면역 반응을 평가할 수 있습니다.
Nachman은 성인의 코로나 바이러스가 어린이의 무증상 감염에 노출되기 전에 선행 될 수 있기 때문에 가족 전체를 치료하기위한 백신을 마련하는 것이 "집과 지역 사회에서 전파를 차단하는 데 큰 도움이 될 수 있습니다"라고 말합니다.
시카고에있는 Weiss Memorial Hospital의 부의장 인 Suzanne Pham, MD는 Verywell에게 아이들이 더 빨리 예방 접종을받을 수 있고 더 빨리 감염률이 감소 할 것이라고 말합니다.
"어린이들에게 효과적으로 예방 접종을함으로써 지역 사회 내에서 어린이들이 바이러스를 전염시킬 위험이 감소 할 것입니다. 특히 중증 또는 중병에 더 취약한 고위험 사람들에게"Pham은 Verywell에 말합니다. “이를 통해 학교는 재개를 시작하고 우리 아이들의 발달에 필수적인 활동을 통제 된 방식으로 재개 할 수 있습니다. 아이들에게 예방 접종을하지 않으면이 바이러스의 확산을 극복 할 수 없습니다. 우리는 사회에서 확산을 막을 수있는 충분한 무리 면역을 가져야합니다.”
COVID-19 백신 : 어떤 백신이 사용 가능한지, 누가 백신을 맞을 수 있는지, 얼마나 안전한지 최신 상태로 유지하십시오.
백신 시험은 어떻게 시작됩니까?
Pham은 성인이나 어린이를 대상으로 백신을 테스트하려면 먼저 IND (Investigational New Drug) 신청서를 FDA에 제출해야한다고 설명합니다.
응용 프로그램은 백신, 제조 방법 및 사용할 품질 관리 테스트를 설명합니다. 이 애플리케이션에는 백신이 인간의 초기 테스트에 안전하다는 것을 입증하는 동물 테스트 데이터도 포함됩니다.
FDA가 설명했듯이 신청 절차에는 여러 단계가 있습니다.
신약의 초기 전임상 개발 기간 동안 스폰서의 주요 목표는 제품이 사람에게 처음 사용하기에 합리적으로 안전한지, 화합물이 상업적 개발을 정당화하는 약리학 적 활성을 나타내는 지 확인하는 것입니다.
제품이 추가 개발을위한 실행 가능한 후보로 식별되면 후원자는 제품이 제한된 초기 단계 임상 연구에 사용될 때 인간이 불합리한 위험에 노출되지 않도록하는 데 필요한 데이터와 정보를 수집하는 데 집중합니다.
그런 다음이 백신은 1 상 시험을 거치게되는데, Pham은 "면밀하게 모니터링되는 소수의 인간 대상을 대상으로 한 안전성 및 면역 원성 연구"라고 설명합니다.
Pham은“2 단계는 용량 범위 연구로 구성되며 더 많은 수 (수백)의 인간 피험자로 확장됩니다. "그런 다음 3 상 시험에서는 수천 명의 인간 피험자를 등록하여 유효성을 문서화하고 안전 데이터를 계속 조사합니다."
웹 사이트에 따르면 Pfizer는 연구에 39,000 명 이상의 자원 봉사자를 등록했습니다. 그들 중 34,000 명 이상이 2 차 접종을 받았습니다.
이것이 당신에게 의미하는 것
어린이를 대상으로 한 COVID-19 백신 테스트를 포함하는 임상 3상은 진전의 신호입니다. 그러나 백신은 서두르지 않습니다. 최종 결과를 확정하는 데는 최종 백신을 맞을 성인과 어린이뿐만 아니라 시험 참가자의 안전을 보호하는 데 시간이 걸립니다.
-may-dampen-the-antibody-response-to-covid-19-vaccines.jpg)